AD治療薬を開発中止~またもIII相試験の壁崩せず
エーザイは、米バイオジェンと共同開発中の自社創製の早期アルツハイマー病(AD)を対象とした経口βサイト切断酵素(BACE)阻害剤「エレンベセスタット」の二つの国際共同第III相試験を中止すると発表した。独立安全性データモニタリング委員会(DSMB)が安全性評価を行った結果、試験を継続しても最終的にベネフィットがリスクを上回ることはないと判断。試験中止を勧告したことから、両社は開発中止を決めた。試験結果の詳細は、今後の学会で発表する予定。同剤の第II相試験「202試験」の長期継続投与試験も中止する。
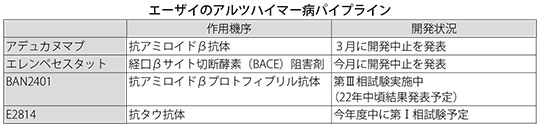
両社は、AD治療薬3剤に関する共同開発・販売契約を結んでいたが、3月にも抗アミロイドβ抗体「アデュカヌマブ」の開発中止を発表している。さらに今回、エレンベセスタットの試験中止を受け、現在進行中の第III相試験は、抗アミロイドβブロトフィブリル抗体「BAN2401」のみとなった。
エレンベセスタットは、エーザイが創製し、大型化を期待していた抗認知症薬。アミロイドβ産生に関わる重要な酵素BACEを阻害することで、アミロイドβの産生を低下させ、脳内のアミロイドプラーク形成を減少させることにより、ADの進行を抑える疾患修飾作用を発揮するとしていた。
早期AD患者2100人を対象とした国際共同第III相試験は、プラセボとの比較でエレンベセスタットの認知機能改善効果や安全性を検討していたが、DSMBがエレンベセスタット投与による患者のベネフィットがリスクを上回るものではないと判断し、試験中止を勧告。両社は、エレンベセスタットの試験中止を決めた。
AD治療薬の開発をめぐっては、米メルク、米イーライリリー、スイスのロシュなどが試験中止を発表し、失敗事例が相次いでいる。エーザイは、2025年までの中期経営計画で、癌と中枢の二つの領域に経営資源を集中させ、中枢では後期段階にあるAD治療剤3剤を成長ドライバーに位置づけていたが、二つの開発候補品が脱落することになった。
同社は、今回のエレンベセスタットの第III相試験中止を受け、「アミロイドβ仮説を否定するものではない」(エーザイPR部)とし、BAN2401の第III相試験を引き続き継続する方針だが、今後の事業計画に大きな影響を与えるのは必至の情勢だ。
出典:薬事日報












薬+読 編集部からのコメント
米メルク、米イーライリリー、スイスのロシュなどが試験中止を発表し、失敗事例が相次いでいる早期アルツハイマー病(AD)治療薬開発事業ですが、日本のエーザイも米バイオジェンと共同開発中の抗認知症薬「エレンベセスタット」の二つの国際共同第Ⅲ相試験の中止を発表しました。両社は3月にも抗アミロイドβ抗体「アデュカヌマブ」の開発中止を発表しています。今回の中止を受け、現在進行中の第Ⅲ相試験は、抗アミロイドβブロトフィブリル抗体「BAN2401」のみとなりますが、引き続き継続する方針です。