後発品111品目を薬価収載~「フェブリク」に13社参入【厚生労働省】
厚生労働省はきょう17日、後発品111品目を薬価基準に収載する。初の後発品収載は、痛風治療剤の「フェブキソスタット」(先発品名:フェブリク錠)など12成分20規格85品目。先発品メーカーから特許使用の許可を得て後発品として発売するオーソライズドジェネリック(AG)の収載は、初後発に限ると利尿剤の「トルバプタン」(先発品名:サムスカ)など4成分6規格6品目が収載された。
今回、薬価収載の希望品目は129品目だったが、安定供給上の不安などを理由に8品目が取り下げられ、最終的に31社28成分45規格111品目が収載された。1998年以降で見ると、111品目は過去4番目に少ない収載品目数となった。
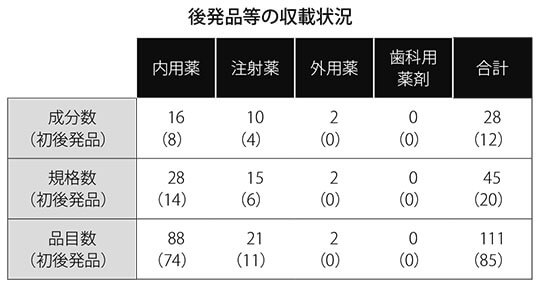
収載状況の内訳を見ると、内用薬が16成分28規格88品目、注射薬が10成分15規格21品目、外用薬が2成分2規格2品目となった。
初めて収載された後発品は、痛風治療剤のフェブキソスタット、抗悪性腫瘍剤のダサチニブ、利尿剤のトルバプタン、高脂血症用剤のオメガ-3脂肪酸エチル、鎮痛剤のトラマドール塩酸塩、カルニチン欠乏症治療剤のレボカルニチン、月経困難症治療剤のドロスピレノン・エチニルエストラジオール・ベータデクス、ラメルテオン、ベンダムスチン塩酸塩水和物など12成分20規格85品目。内用薬が8成分14規格74品目、注射薬が4成分6規格11品目で、外用薬はなかった。
このうち、AGは4成分6規格6品目が収載される。内訳は、オメガ-3脂肪酸エチル1規格1品目、トルバプタン1規格1品目、フェブキソスタット3規格3品目、ラメルテオン1規格1品目だった。
医療安全の観点から一般名に変更したなどの代替新規を含め、収載品目数が多かった上位企業は、沢井製薬と東和薬品が13品目と最多となり、次いでニプロファーマ7品目、あすか製薬、日新製薬、日本ケミファ、MeijiSeikaファルマが6品目の順となった。
代替新規を除いた収載品目数の上位企業は、東和薬品13品目、沢井製薬11品目、ニプロファーマ7品目、日新製薬、日本ケミファ、MeijiSeikaファルマの6品目だった。
収載品目数が最も多かったのは、フェブキソスタットの13社50品目、次いでダサチニブの4社8品目となった。
新規収載希望が10品目を超えた内用薬を先発品の「0.4がけ」とするルールは、フェブキソスタットの1成分3規格50品目に適用された。
出典:薬事日報
















薬+読 編集部からのコメント
6月17日、厚生労働省は後発品111品目を薬価基準に収載しました。初の後発品収載となったのは痛風治療剤の「フェブキソスタット」(先発品名:フェブリク錠)など12成分20規格85品目。
薬価収載の希望品目は129品目でしたが、安定供給上の不安などを理由に31社28成分45規格111品目が収載され、1998年以降で見ると過去4番目に少ない収載品目数となりました。